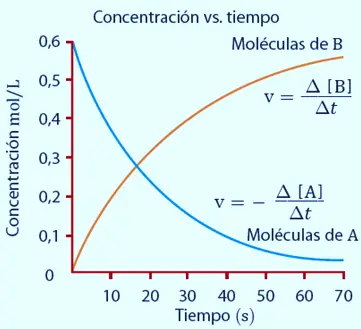
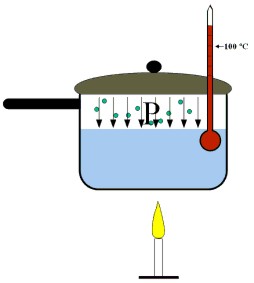
Depende de varios factores como la concentración de los reactivos, la presencia de un catalizador, la temperatura de reacción y el estado físico de los reactivos.
La velocidad de una reacción química no ocurre de la misma forma, algunas reacciones se producen de manera instantánea y otras transcurren lentamente.
Factores que influyen en la rapidez de la reacción:
- Temperatura a la cual se desarrolla la reacción.
- Grado de división de los reactivos.
- Naturaleza de los reactivos.
- Concentración de los reactivos.
- Catalizador si lo hubiera.